Exkurs: Das asymmetrische Kohlenstoffatom
Um den historischen Weg
kennen zu lernen, vergleichen Sie bitte Bromchlorfluormethan und
Bromchlormethan:
 |
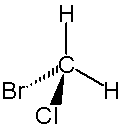 |
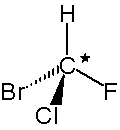
| Bromchlorfluormethan | Bromchlormethan |
Mit ihrem Wissen über Symmetrieelemente erkennen Sie sofort, dass Bromchlorfluormethan keines
der geforderten Symmetrieelemente besitzt: es muss daher chiral sein.
Bei Bromchlormethan geht eine innere Spiegelebene durch das Molekül
(Ebene Br-C-Cl). Die Liganden Brom und Chlor liegen in der Ebene und werden auf sich selbst abgebildet,
die beiden Wasserstoffliganden können aufeinander gespiegelt werden. Das Molekül ist achiral.
Nach dem historischen Weg müsste man wie folgt vorgehen:
Ein Molekül ist dann chiral, wenn ein Kohlenstoffatom mit vier verschiedene Substituenten vorkommt.
Bsp.: Im Fall von Bromchlorfluormethan ist dies mit den Liganden Br, Cl, F und H gegeben. Ganz anders bei Bromchlormethan: da sind es nur drei verschiedene Liganden, Br, Cl und (zweimal) H.
Ein Atom mit vier verschiedenen Liganden bezeichnet man demnach als Chiralitätszentrum (nach Prelog, 1956), stereogenes Atom (nach Mislow), Stereozentrum oder "asymmetrisches Atom" (nach van't Hoff, 1874). Es wird oft durch einen Stern (*) gekennzeichnet.
Demnach müssten wir folgern:
|
Moleküle mit einem Chiralitätszentrum sind chiral. |
Wie irreführend das ist, zeigt eine Lehrbuchzitat auf der nächsten Seite...