Seminar zur Didaktik der Chemie I, WS 2003/04 Planungs- und Arbeitsphasen
1. Einführung und ProblembewusstseinAusgangspunkt ist die im Vorjahr konzipierte zweite UE zum experimentellen Erstkontakt von Schülern im Fach Chemie. Im Verlauf mehrerer Jahre soll eine Sequenz experimentbasierter Unterrichtseinheiten entstehen, die stets von Erfahrungen mit den Stoffen ausgehend die theoretischen Grundlagen vermitteln soll. Aufgabe dieser Einheit wird sein, die Plattform zu definieren, auf deren Grundlage eine Erklärung der bisher beobachteten Phänomene des Mischens und der chemischen Reaktion vorgenommen werden können. 1.1 Erste Annäherungsphase: Aus den verschiedenen Richtungen soll ein Situationsbericht entstehen:
Das Teilchenkonzept (Diskontinuumkonzept) wird allgemein und (im Unterricht) kaum hinterfragt eingeführt. Finden wir eine klare Begründung für die Notwendigkeit von Teilchen oder ist die Alltagserfahrung des Kontinuums auch für das Fach Chemie in der Schule ausreichend? Die in Becker et. al. Fachdidaktik Chemie beschriebene Situation in den 80er Jahren, "der wissenschaftliche Chemieunterricht" habe "die mit dem Diskontinuum verbundenen Probleme noch nicht bewältigen können" besteht nach wie vor. Lösungsvorschläge sind:
Als Lernschwierigkeiten wird
1.2 Zweite Annäherungsphase.1.2.1 Die Frage nach dem Zweck: wozu brauchen wir ein Teilchenkonzept? Antworten gemäß Lehrplaninhalten:
1.2.2 Die Frage nach der problemhaften Notwendigkeit: Wir sehen nur zwei Gründe, aus denen sich auch für den Lernenden die Notwendigkeit der Diskontinuumssicht ergeben könnte:
2. Erarbeitungsphase2.1 Die Situation. In den Aussagen des Lehrplans und der Schulbücher (Elemente der Zukunft: Chemie 1, Natur und Technik: Chemie 9) findet sich keine Begründung des Teilchenaufbaues. Das Bohrsche Atommodell wird als einziges Modell unbegründet eingeführt. Von den häufigeren Modellen werden folgende auf Eignung diskutiert:
Kugelwolken- und VSEPR-Modell sind demnach besser geeignet als die Bohrschen Schalen, wobei das VSEPR-Modell besonders beim Molekülbau die besten Leistungen zeigt, also in einem Bereich, der kaum realschulrelevant ist. Deshalb fällt die Entscheidung auf das Kugelwolkenmodell. Schüler könnten folgende Alltagsbeobachtungen gemacht haben, die eine Kontinuumssicht suggerieren:
Beobachtungen mit Hilfsmitteln sind selten, so dass die Feststoff-Partikel im Rauch nicht wahrgenommen werden. Aus Lösungen kann das der Stoff durch Verdunsten des Lösungsmittels wieder dargestellt werden - an sich ein Grundschulexperiment im HS-Unterricht. Es beweist aber lediglich, dass Materie durch Auflösen nicht vernichtet worden ist, nicht die Teilchennatur. Schließlich ist die Teilchennatur des Wasserdampfes experimentell nicht direkt zugänglich: Kondensation beweist wie vorhin nur, dass das Wasser nicht im Nichts verschwunden ist. Auch die meisten Erwachsenen (einschließlich mancher Naturwissenschaftslehrer) bezeichnen Dunst über siedendem Wasser als Wasserdampf und nicht als Nebel. 2.2 Ansätze zur Lösung. In jeweils 2-3 Arbeitsgruppen werden Konzepte für eine mehrstündige Unterrichtseinheit skizziert, dann diskutiert und die interessantesten Ansätze ausgewählt. Aus der Synthese entsteht folgende Skizze für den Umfang von ca. 5 Unterrichtsstunden:
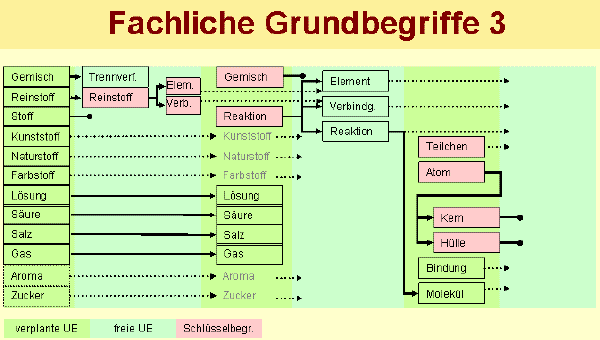
2.3 Stand der Grundbegriff-Verteilung
3. LösungUnterrichtseinheit zum Thema "Teilchenaufbau der Materie".
E-Mail: Walter.Wagner ät uni-bayreuth.de |