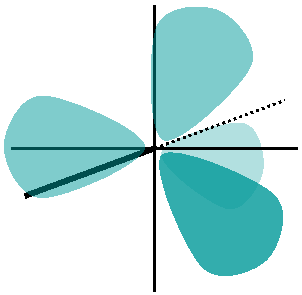sp3-Hybridorbitale |
||||
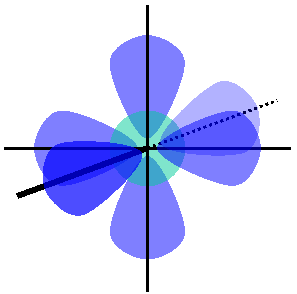
Durch Linearkombination von einem s- und drei p-Orbitalen derselben Schale entstehen vier ‰quivalente sp3-Hybridorbitale. Man sagt dann, das Atom sei sp3-hybridisiert. Die sp3-Hybridorbitale stehen im Winkel von 109∞28' zueinander; sieht man das sp3-hybridisierte Atom als Zentrum an, stehen sie in den Ecken eines Tetraeders. Die sp3-Hybridisierung erkl‰rt z. B. die Vierbindigkeit des Kohlenstoffs.
|
||||
| (c) Walter.Wagner ‰t uni-bayreuth.de, Universität Bayreuth; Impressum |