|
Hintergrund zu:
Alkalimetalle in Wasser
Eigenschaften der Alkalimetalle Die
Alkalimetalle bilden eine homogene Gruppe auÔerordentlich reaktiver
Elemente, die beispielhaft die áhnlichkeiten und Tendenzen illustrieren,
welche durch die periodische Klassifizierung erwartet werden k—nnen. Ihre
physikalischen und chemischen Eigenschaften lassen sich zwanglos auf der
Grundlage ihrer einfachen Elektronenkonfiguration ns1
interpretieren.
Es sind alles weiche, niedrig schmelzende, silbrig-weiÔe Metalle, die mit
kubisch raumzentrierten Gittern kristallisieren. [1]
| Element |
Lithium |
Natrium |
Kalium |
Rubidium |
Caesium |
| |
griech. lithos = Stein |
hebr. neter = Soda |
arab. al kalja = Pflanzen- asche |
lat. rubidus = dunkelrot |
lat. caesius = himmel- blau |
| Symbol |
Li |
Na |
K |
Rb |
Cs |
| relative Atommasse [u] |
6,941 |
22,9898 |
39,0983 |
85,4678 |
132,905 |
| Schmelzpunkt [¯C] |
179,0 |
97,8 |
63,5 |
39,0 |
28,5 |
| Siedepunkt [C¯] |
1340 |
883 |
760 |
696 |
708 |
| Hðrte |
abnehmend
 |
| Hðufigkeit Erdkruste [%] |
6,0*10-3 |
2,63 |
2,41 |
2,9*10-2 |
6,5*10-4 |
| Flammen-fðrbung |
karminrot |
gelb |
violett |
dunkelrot |
hellblau |
| Reaktions-fðhigkeit |
zunehmend
 |
| Stðrke der Lauge |
zunehmend
 |
| Atomradius [pm] |
152 |
186 |
227 |
248 |
265 |
| EN nach Alfred/Rochow |
0,97 |
1,01 |
0,91 |
0,89 |
0,86 |
| 1.Ionisierungs-energie [eV] |
5,39 |
5,14 |
4,33 |
4,18 |
3,89 |
| Normal-potential [V]
|
-3,045 |
-2,714 |
-2,925 |
-2,925 |
-2,923 |
| Hydratations-enthalpie [kJ/mol] |
-508 |
-398 |
-314 |
-289 |
-256 |
F■r die chemische Reaktivitðt ist vor allem die H—he
der Elektronegativitðt und die Anzahl der Valenzelektronen
ausschlaggebend. Die Alkalimetalle besitzen nur 1 Valenzelektron, durch
dessen Abgabe sie die Edelgaskonfiguration erreichen k—nnen. Daher sind
die Ionisierungsenergien der Alkalimetalle besonders niedrig. Mit
abnehmender Elektronegativitðt steigt die Reaktivitðt der Alkalimetalle,
d.h. ihre Fðhigkeit Elektronen abzugeben. [3][2] Die Reaktion mit Wasser
Entsprechend dem mit steigender Atommasse zunehmenden elektropositiven
Charakter nimmt die Reaktivitðt der Alkalimetalle gegen■ber Wasser vom
Lithium zum Kalium zu. Lithium scheint bei diesem Versuch heftiger und
schneller zu reagieren als Natrium. Dies liegt wahrscheinlich an der
besonders hohen Hydratationsenthalpie des Lithiumions (dHR = -
508kJ/mol), welche die Bildung von Li+-Ionen in wðssriger
L—sung und somit die Reaktion beg■nstigt. [4][2]
Bei dieser Reaktion kommt es zur Hydroxid- und Wasserstoffbildung,
sowie teilweise zur Verbrennung der Alkalimetalle.
Bildung von Hydroxiden
 | Lithium reagiert mit Wasser unter Bildung von Lithiumhydroxid, ohne zu schmelzen und ohne Entz■ndung
des Wasserstoffs. Dies ist wahrscheinlich auf die
h—here Reaktionsenthalpie von Lithium zur■ckzuf■hren:
 |
 | Natrium schmilzt bei der Reaktion (Schmelzpunkt 98¯C), ohne dass der Wasserstoff
verbrennt (bei freier Beweglichkeit des Metalls):
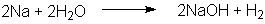 |
 | Kalium (sowie auch die schwereren Alkalimetalle) schmilzt und reagiert so heftig,
dass sich der gebildete Wasserstoff entz■ndet:
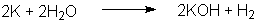 .
[4] .
[4] |
Nachweis der gebildeten Hydroxide
Bei der Reaktion mit Wasser bilden die
Alkalimetalle die basischen Hydroxide. Diese l—sen sich in Wasser unter starker
Erwðrmung und bilden Laugen. Mit einem Sðure-Base-Indikator kann der Umschlag ins
basische nachgewiesen
werden.
In diesem Versuch wurde der Indikator Neutralrot verwendet (siehe Abb.1). [3]
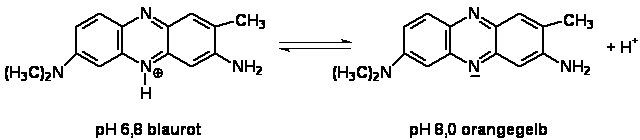
Abb.1: Neutralrot [7]
Wasserstoffentwicklung
Durch die stark negativen Normalpotentiale der Alkalimetalle wird Wasser [E(H+/H2) = 0,42V bei pH=7] unter Bildung von Wasserstoff reduziert. Der aus dem Rahmen fallende hohe negative Wert des Normalpotentials
von Lithium ist wahrscheinlich auf die besonders hohe Hydratationsenthalpie des Lithiumions zur■ckzuf■hren, welche die Bildung von Li+-Ionen in wðssriger
L—sung beg■nstigt.
Kalium zersetzt Wasser mit so groÔer Heftigkeit, dass die entstehende
Wðrme gen■gt, um den gebildeten Wasserstoff zu entz■nden. Es kann auch ein
Knall entstehen, wenn sich Wasserstoff mit dem Luftsauerstoff zu
Knallgas (H2:O2= 2:1) vermischt
(Knallgasreaktion).
Die starke Wasserstoffentwicklung und der Effekt des siedenden Wassers
bewirken die Bewegung des Metalls. [4]
Verbrennung des Alkalimetalls
Die Alkalimetalle bilden eine faszinierende Vielfalt von binðren
Verbindungen mit Sauerstoff. Das vielseitigste ist Cðsium, das 9
Verbindungen mit St—chiometrien vom CsO7 bis zum CsO3
bildet .
Werden die Metalle unter ausreichen Luftzufuhr verbrannt, so ist das
jeweilige Hauptprodukt vom eingesetzten Metall abhðngig: Lithium bildet das
Oxid Li2O (und etwas Li2O2), Natrium gibt das Peroxid Na2O2 (und etwas Na2O),
wohingegen Kalium, Rubidium und Cðsium das Hyperoxid MO2 bilden. [1]
Lithiumoxid:
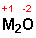
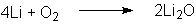
Natriumperoxid:
Gegen■ber getrockneten Sauerstoff ist Natrium sehr bestðndig. So
kann es in vollkommen trockenem Sauerstoff geschmolzen werden (Smp. 98¯C),
ohne sich zu entz■nden. Bei Anwesenheit von Spuren Feuchtigkeit verbrennt
es dagegen beim Erwðrmen an der Luft leicht mit intensiv gelber Flamme.
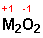

Mit oxidierbaren Stoffen kann es unter Explosion reagieren!
Kaliumhyperoxid:
K verbrennt beim Erhitzen an der Luft leicht mit intensiv violettem Licht
zu Hyperoxid.:
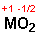
 .[5]
.[5]
Genaue Informationen sowie die MO-Schemata zu den Oxiden, Peroxiden, Hyperoxiden der Alkalimetalle
unter:
http://www.uni-bayreuth.de/departments/didaktikchemie/umat/alkalimet_overb/alkalimet_overb.htm
Peroxide und Oxide der Alkalimetalle Kalium, Rubidium und Cðsium
sind ebenfalls bekannt. Sie entstehen durch "kontrollierte Verbrennung", d.h. es darf nur die st—chiometrisch exakte Sauerstoffmenge zur
Verf■gung gestellt werden. [6]
Verwendungsm—glichkeiten der Alkalimetalle
| Element |
Verwendung |
| Li |
 | Li gibt als Legierungsbestandteil Hðrte und Bestðndigkeit ;
z.B.
Bahnmetall der Deutschen Bundesbahn : Pb/Ca/Na/Li (0,04%).
|
 | Das Isotop 6Li wird zur Herstellung von 3H
verwendet |
 | Verwendung als Anode in Sekundðrzellen |
 | Darstellung von Lithiumorganylen
|
 | Lithiumcarbonat hat in kleinen Dosen eine
antidepressive Wirkung |
|
| Na |
 | Verwendung zur Herstellung von Spezialmetallen,
z.B. Titan
|
 | Vitamin A -Herstellung und Indigoreduktion .
|
 | Zerst—rung halogenorganischer Verunreinigungen in Fl■ssigkeiten.
|
 | Na/S-Hochleistungsbatterie f■r Elektrofahrzeuge.
|
 | Fl■ssiges Natrium dient aufgrund seiner guten Wðrmeleitfðhigkeit
als K■hlmittel in Kernreaktoren oder als Wðrme■bertrðger in
Kraftwerken |
|
| K |
 | 40K
ist radioaktiv und eignet sich zur Altersbestimmung von Mineralien
|
 | Hauptsðchlich Verwendung der Salze als D■ngemittel.
Die nat■rlichen Kaliumsilikate k—nnen von den Pflanzen nicht gut
genutzt werden. Zur D■ngung werden daher bei intensiver
Bewirtschaftung KNO3 , K2SO4 oder KCl
verwendet. |
|
| Rb/Cs/Fr |
 | Rubidiumsalze wie Rubidiumchlorid oder Rubidiumbromid werden in
der Medizin als Schmerz- oder Beruhigungsmittel eingesetzt. |
 | 137Cs
dient wegen seiner kurzen Halbwertszeit (33 Jahre) zur Herstellung
technischer Gamma-Strahlenquellen.
|
 | Braunschweiger Cðsiumuhr (seit 1978) verwendet 133Cs
Derartige Uhren weichen in 10000 Jahren nur 0,3 Sekunden ab.
|
|
. [2][3]
Literatur:
- Greenwood, N.N., Earnshaw, A.: Chemie der Elemente, 1. korrigierter Nachdr.
d. 1. Aufl., VCH, Weinheim, Basel, Cambridge, New York, 1990, S. 83-111
-
http://www.seilnacht.com/Lexikon/19Kalium.htm, 22.02.06
-
http://www.uni-bayreuth.de/departments/didaktikchemie/
umat/alkalimet/alkalimetalle.htm. 22.02.06
-
http://www.cci.ethz.ch/vorlesung/de/al2/node2.html, 22.02.06
- Holleman, A.F., Wiberg, E.: Lehrbuch der Anorganischen Chemie, 81.-90.
Aufl., Walter de Gruyter, Berlin, New York, 1976, S. 707-740
-
http://www.uni-bayreuth.de/departments/didaktikchemie/
umat/alkalimet_overb/alkalimet_overb.htm, 22.02.06
- Falbe, J., Regitz, M.: R—mpp Chemie Lexikon, 9. Aufl., Georg Thieme
Verlag, Stuttgart, New York, 1991, S. 2979
|
ˋ Walter.Wagner ðt uni-bayreuth.de,
Stand:
20.09.10
|