Hintergrund zu:
Das oszillierende Platinherz
Die Temperatur des Platindrahts reicht nicht aus, um den
Methanoldampf im Erlenmeyerkolben zu entzünden (Zündpunkt: 455°C) [1]. Jedoch läuft auf der Oberfläche des Platindrahtes eine
katalysierte Verbrennung des Methanols ab, die eine niedrigere
Aktivierungsenergie erfordert. Diese heterogene Katalyse ist endotherm:
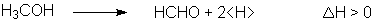
Die so gebildeten Wasserstoffatome verbinden sich nicht zu
Wasserstoffmolekülen, sondern werden von der Oberfläche des
Platindrahtes adsorbiert. Mit der Luft gelangen
Sauerstoffmoleküle in den Erlenmeyerkolben. Diese
Sauerstoffmoleküle reagieren an der Oberfläche des Platindrahtes mit den dort adsorbierten Wasserstoffatomen zu
Wassermolekülen, die in Form von Wasserdampf abdiffundieren:
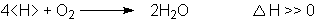
Diese Reaktion
(Knallgasreaktion) ist so stark exotherm, dass der
Platindraht eine Temperatur von etwa 1000°C erreicht und dadurch
hellrot erglüht.
Die frei werdende Reaktionswärme der zweiten Reaktion liefert die
Reaktionswärme für die erste Reaktion und hält trotz hoher
Energieabgaben an die kalte Umgebung den Platindraht am Glühen.
Sobald im Erlenmeyerkolben ein verpuffungsfähiges Gemisch aus
Luft, Methanoldampf und Formaldehyd erreicht ist, zündet der
glühende Platindraht dieses Gasgemisch. Bei der Verpuffung laufen zwei Oxidationsreaktionen ab:
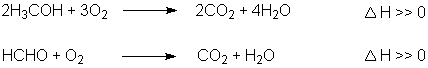
Die Verpuffung wird akustisch
von einem Geräusch und visuell von einer blau flackernden Flamme
begleitet. Kurzfristig besteht danach die Gasatmosphäre im
Zylinder aus den Reaktionsprodukten der Verpuffung: Wasserdampf
und Kohlenstoffdioxid.
Die katalytische Reaktion am Platindraht wird durch den Mangel
an Sauerstoff als Folge der
Verpuffung für wenige Sekunden unterbrochen, wodurch der Draht zu
glühen aufhört. Neu einströmender Sauerstoff startet die
katalysierte Reaktion an der Oberfläche des Platindrahtes jedoch
erneut. Sobald der Platindraht ca. 455°C erreicht, entzündet er
das entstandene Gasgemisch im Erlenmeyerkolben erneut. Der Prozess wiederholt sich so lange, bis das Methanol
verbraucht ist. [2]
Literatur
- www.experimentalchemie.de/versuch-012.htm,
Stand 14.12.05
- Nick,
S., Parchmann, I., Demuth, R.: Chemisches Feuerwerk - 50 effektvolle
Schauversuche, 1. Aufl., Aulis Verlag Deubner, Köln, 2001, S.173-179