Hintergrund zu:
Goldstaub
Bei der Reaktion von Bleisalzen mit Kaliumiodid fällt aus der zuvor
farblosen Lösung ein sattgelber Niederschlag - das Bleiiodid - aus. Es
kommt zur Ausbildung eines chemischen Gleichgewichtzustandes zwischen dem
festen Bleiiodid
und den Ionen:
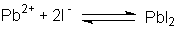
Zur Verdeutlichung der Einstellung eines Löslichkeitsgleichgewichtes
gibt man zur Lösung, die bei der Bleiiodid-Herstellung
angefallen ist, einige Tropfen Kaliumiodid-Lösung. Es fällt erneut
eine erstaunlich große Menge an Bleiiodid aus. Dieser Vorgang wird auch
als Nachfällen bezeichnet. Das Phänomen kann dadurch erklärt werden,
dass bei der Herstellung von Bleiiodid nicht alle Blei- und
Iodidionen miteinander unter Bildung von Bleiiodid-Kristallen reagiert
haben, sondern in Lösung geblieben sind.
Durch Temperaturerhöhung wird der Gleichgewichtszustand zu den Blei-
und Iodidionen hin verschoben. Das gelbe Bleiiodid löst sich auf, wodurch
die Lösung farblos erscheint.
Bleiiodid ist nur als Festkörper sattgelb. Der Grund ist, dass die
Bleiionen die Elektronenschale der großen, voluminösen Iodidionen so
beeinflussen, dass sie schon durch sichtbares Licht angeregt werden
können. Sie absorbieren aus dem weißen Licht folglich blaues Licht;
sichtbar ist gelb.
Literatur:
-
http://dc2.uni-bielefeld.de/dc2/tip/04_02.htm, Stand 20.02.06