|
Herstellen einer
organischen Solarzelle
(Grštzel-Zelle)
Erklšrung
|
L |
HerkŲmmlichen Solarzellen bestehen im
Wesentlichen aus Silizium: es liefert bei Sonneneinstrahlung die Elektronen und
diese kŲnnen, dank der elektrischen Leitfšhigkeit von Silizium, zu den
Elektroden flieŖen.
In der Grštzel-Zelle gibt es fŁr die beiden
Aufgaben zwei verschiedene Stoffe:
-
ein (organischer) Farbstoff liefert bei
Lichteinstrahlung die Elektronen und
-
Titandioxid leitet sie zu den Elektroden.
Erklšrungsebene Jgst. 5-11:
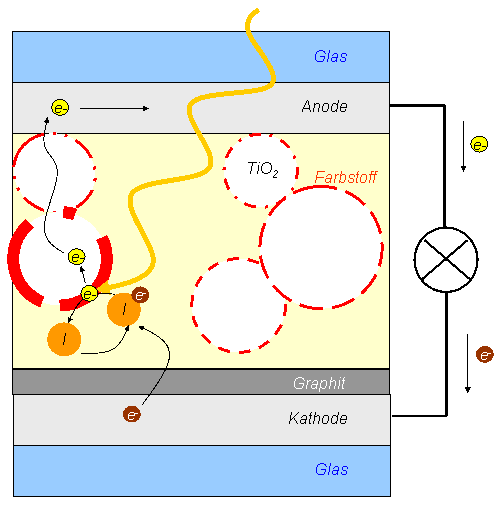
Abb. 1: Schematischer Weg der
Elektronen
schnelle Animation (PowerPoint
XP erforderlich: ppt 4,5M
schrittweise Animation (PowerPoint XP erforderlich: ppt
4,5M
Erklšrungsebene Jgst. 12-13:
Durch die Absorption eines Photons wird aus dem
FarbstoffmolekŁl ein Elektron freigesetzt und durch das elektrisch leitende Titandioxid zur Anode abgefŁhrt.
Nun muss dafŁr
gesorgt werden, dass die Elektronen auf ihrem Weg nicht wieder zu den
ionisierten Farbstoff-MolekŁlen Ąumkehrenď, da es dann keinen Stromfluss geben
wŁrde. Aus diesem Grunde fŁgt man einen Elektrolyten bei, der dem Farbstoffkation schnell ein Ersatzelektron nachliefert, hier
Iod-Kaliumiodid-LŲsung.
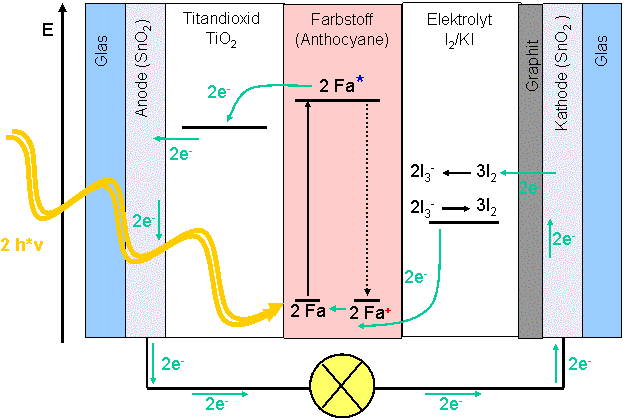
Abb. 2: Redox-Vorgšnge und
Schichtenaufbau
Animation (PowerPoint XP erforderlich: ppt 4,5M
In Schritten:
-
Durch einfallende Lichtstrahlen (Quanten) werden in den
Farbstoff-MolekŁlen Fa Elektronen energetisch angeregt und durch deren Energie auf ein hŲheres
Energieniveau gebracht.
Fa + hv --> Fa*
-
Da sich das Energieniveau oberhalb der Leitungsbandes
von
Titandioxid befindet, kann das Elektron Łbertreten (ein wenig "herunterfallen"):
aus dem angeregten Zustand der
Farbstoff-MolekŁle werden die Elektronen auf das Leitungsband des Titandioxids
Łbertragen.
Ox.: Fa* --> Faox + e-
Leitung: TiO2 + e- --> TiO2-
TiO2-
--> TiO2 + e-
Dieser Ladungsinjektion entgegen stehen Deaktivierungsprozesse. Mit ausgewšhlten Farbstoffen
erzielt man heute bereits Ausbeuten von etwa 90 %.
-
Aus der Anode flieŖen die Elektronen Łber den
Verbraucher, der die zugefŁhrte Energie "verbraucht" (eigentlich: umwandelt),
zur Kathode.
-
Die Kathode fŁhrt diese Elektronen dem System
zurŁck. Nur deshalb bleibt der Elektronenfluss aufrecht. Zunšchst wird der Elektronenverlust des Farbstoffs
aus dem Iodid der
Elektrolyt-LŲsung ausgeglichen, indem es zu Triiodid reduziert wird.
Ox.: 3 I- --> I3- + 2e-
Red.:
2 Faox + 2e- --> 2 Fa
-
Dann wird das Iodid mit Hilfe der Elektronen aus
der Kathode zurŁckgebildet:
I3- + 2 e- --> 3 I-
Das System befindet sich wieder in der Ausgangslage.
© Walter.Wagner št uni-bayreuth.de
|

