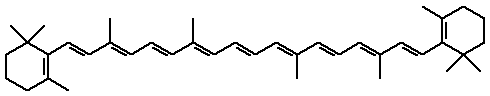
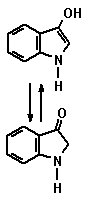1. Farbstoffklassen bei PflanzenDas Charakteristikum aller Farbstoffe ist ihre Fähigkeit, Energie des Teils der elektromagnetischen Strahlung zu absorbieren, der für das menschliche Auge sichtbar ist (400 – 700 nm). Die vom Farbstoffmolekül aufgenommene Energie bringt Elektronen in angeregte Zustände. Der grüne Blattfarbstoff Chlorophyll absorbiert purpurnes Licht der Wellenlänge 730 nm und repräsentiert den wichtigsten Blattfarbstoff, weil er die Photosynthese, also die Umwandlung von Kohlendioxid und Wasser in Glucose und CO2 ermöglicht. Chlorophyll besitzt nur eine geringe Farbstabilität und ist wasserunlöslich. Durch Verseifung und Austausch des Mg2+-Ions durch das Cu2+-Ion entstehen die wasserlöslichen und lichtbeständigeren Chlorophylline, die als Lebensmittelfarbstoff zum Färben von Getränken, Gummibärchen oder grünen Nudeln verwendet werden. Wenn man sich fragt, worauf die rote Farbe von Karotten und Tomaten, die tiefblaue Blütenfarbe der Kornblume und des blauschwarzen Stiefmütterchens oder aller anderen wunderschönen Blütenfarbstoffe zurückzuführen sind, kommt man im Wesentlichen zu fünf Naturfarbstoffklassen. 1.1 CarotinoideCarotinoide wie Beta-Carotin verleihen Tomaten und Karotten die rote Farbe. Aus Karotten werden sie auch technisch gewonnen und zur Färbung von Getränken eingesetzt.
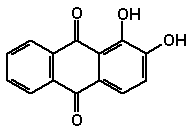
Beta-Carotin 1.2 AnthrachinoneAlizarin kommt in der Krappwurzel vor und gehört zu den Anthrachinonen. Es ist verantwortlich für die karminrote Färbung von Textilien mit dieser Droge.
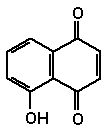
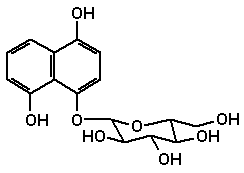
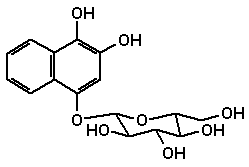
1.3 1,4- NaphthochinoneDas Glucosid von Hydrojuglon wird in den Blättern des Walnussbaumes (Juglans regia L.) gebildet und gelangt entweder über die Wurzeln oder herabgefallene Blätter in den Boden. Dort wird es mikrobiell hydrolysiert, also das Glucosid gespalten und anschließend das gebildete Hydrojuglon oxidiert. Das entstandene Juglon unterdrückt die Keimung und das Wachstum zahlreicher Pflanzenarten. Dieser allelopathische Effekt ist der Grund dafür, dass unter Walnussbäumen kaum andere Pflanzen wachsen. Juglon und ähnlich strukturierte 1,4-Naphthochinone aus Walnussschalen erlauben eine gelbbraune Färbung von Textilien.
Juglans regia L.[1]
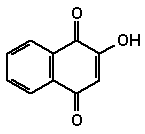
In Hennablättern (Lawsonia inermis L.) kommt das Glucosid von 1,2,4-Trihydroxynaphthalin vor, das nach Hydrolyse und Oxidation das rot färbende Lawson liefert. Dieser Farbstoff wird beispielsweise in Haarwaschmitteln zum Rotfärben verwendet.
Lawsonia inermis L.[2]
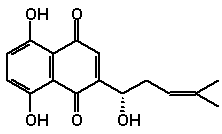
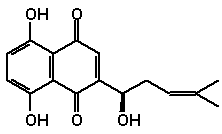
(-)-Alkannin und verwandte Farbstoffe werden aus Alkannawurzeln (Alkanna tinctoria L.) gewonnen und dienen zur Braunfärbung von Lebensmitteln und Kosmetika.
Alkanna tincoria L. [3] Mit dem aus der Pflanze Echter Steinsamen (Lithospermum officinale) erhaltenen (+)-Shikonin werden vor allem in Japan Textilien und Lippenstifte gefärbt.
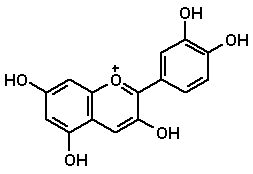
1.4 FlavonoideIn allen Pflanzen kommen gelb bis hellbraun färbende Flavonoide vor. Als Beispiel sei Gartensalbei (Salvia officinalis L.) genannt, der Luteolin und Hyperosid enthält. Zu den Flavonoiden zählen auch die Anthocyane, die ausschließlich in Blüten und Früchten vorkommen. Anthocyane sind für Farben von Blau über viele Nuancen bis zu Rot verantwortlich. Bei den Anthocyanen handelt es sich um Glycoside, deren Aglykone die Chromophore darstellen. Die tiefblaue Blütenfarbe der Kornblume (Centaurea cyanus L.) und des Blauschwarzen Stiefmütterchens ist teilweise auf Cyanidin zurückzuführen. Die Farbe von Cyanidin ist pH abhängig: pH 1 bis 2 rot, pH 6 bis 6,5 rot-violett, pH 11 blau. Im vorwiegend schwach sauren Zellsaft der Pflanze sollte die Farbe rot-violett sein. Die blaue Farbe ist auf einen Komplex zurückzuführen, der aus 6 Cyanin- und Succinylcyanin und 6 Flavonmolekülen sowie 2 Metallionen (Fe3+, Al3+) besteht.
Centaurea cyanus L. [4]
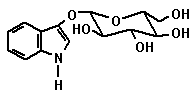
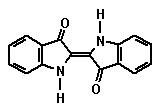
Cyanidin 1.5 IndigoDer blaue Farbstoff Indigo wird aus Färberwaid (Isatis tinctoria L.) und Indigostrauch (Indigofera tinctoria L.) gewonnen. Die in den beiden Pflanzen vorkommenden Glycosylindoxyle Indican und Isatan B werden im Verlaufe des Prozesses der Farbstoffgewinnung hydrolytisch durch bakterielle Enzyme (Enterobacter agglomerans) zu Indoxyl gespalten, das durch Oxidation mit Luft in Indigo übergeht.
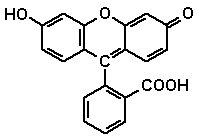
2. Ein synthetischer Farbstoff: FluoresceinDer synthetisch hergestellte Triphenylmethanfarbstoff Fluorescein wird trotz seiner ungeheuren Färbekraft wegen seiner geringen Beständigkeit nicht in der Färberei eingesetzt. Fluorescein liegt im festen Zustand in 2 Formen vor: Stabile rote Kristalle und gelbes amorphes Pulver mit dem Schmelzpunkt 314 – 316°C. Eine Lösung w=1% von Ammoniumfluorescein in Wasser ist rotbraun gefärbt und kaum fluoreszierend, bei Verdünnung 1 : 100.000 (10 ppm) blassgelb und stark grün fluoreszierend und bei Verdünnung 1 : 100.000.000 (0.0001 ppm) ist die Fluoreszenz im Sonnenlicht noch gut wahrnehmbar. Die durch das menschliche Auge wahrnehmbare optische Fluoreszenz ist dadurch gekennzeichnet, dass die Verbindungen 10-10 bis 10-7s nach der Anregung durch sichtbares Licht die absorbierte Energie in Form von Strahlung gleicher oder längerer Wellenlänge wieder abgeben. In der Regel ist Fluoreszenz umso besser zu beobachten, je geringer die Konzentration und je tiefer die Temperatur ist, da Fluoreszenzlöschung durch weniger Stöße zwischen den Farbstoffmolekülen vermieden wird. Mit 500 g Fluorescein können Schiffbrüchige eine Meeresfläche von ca. 4000 m2 auffällig färben. Fluorescein wird in der Medizin zur Diagnose von Hornhauterkrankungen des Auges und in der Kosmetik zum Färben von Seifen und Badezusätzen eingesetzt.
Fluorescein
3. Beispiel eines farbgebenden Prinzips aus dem Tierreich, das auch in der Technik Anwendung findet.Das Insekt des Jahres 2000, der Rosenkäfer, fällt durch seine glänzenden kupfergoldgrünen Flügeldecken sofort ins Auge.
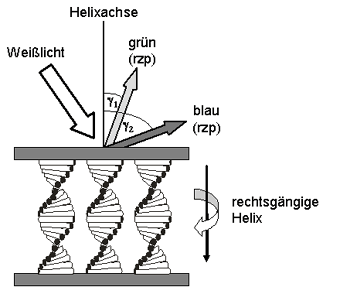
Rosenkäfer, Cetonia aurata [5] Die brillanten Farben werden aber nicht durch Lichtabsorption organischer Moleküle erzeugt, sondern durch Reflexion von sichtbarem Licht. Das Besondere am Rosenkäfer ist, dass seine Flügeldecken zirkular polarisiertes Licht reflektieren.
Rosenkäfer im zirkular polarisierten Licht, [5] Betrachtet man den Käfer durch Zirkularpolarisationsfolien, so erscheint er durch den Rechtszirkularpolarisator schwarz, während durch den Linkszirkularpolarisator die Farben noch brillanter wirken. Die Flügel reflektieren linkszirkular polarisiertes Licht und zwar nur den schmalen gelben bis grünen Bereich des sichtbaren Spektrums. Zusätzlich ändert sich die Farbe je nach dem Betrachtungswinkel von gelb nach grün, was als Farbflop-Effekt bezeichnet wird. Die zirkular polarisierte Lichtreflexion kommt durch Interferenzeffekte zustande, die auf einer helixförmigen Struktur des farblosen Chitins in den Flügeldecken des Rosenkäfers beruht. Die Farbflop-Effekt-Lackierung des Mercedes beruht in Analogie zum Rosenkäfer auf helikalen Strukturen im sogenannten cholesterischen Polymernetzwerk.
Mercedes-Modell mit Farbflop-Lackierung, [6] Die organischen Effektpigmente auf cholesterischer Basis werden von der Firma Wacker-Chemie unter dem Handelsnamen Helicone vertrieben und auch in anderen Bereichen wie Sportartikeln, Spiel- und Lederwaren eingesetzt.
Quellen:
© Walter.Wagner ät uni-bayreuth.de |