
Einführung für Lehrer

Die räumliche Struktur von Kohlenwasserstoffen ist in der Chemie eine
wichtige Grundlage zum Verständnis verschiedener Vorgänge und physikalischer
Eigenschaften. Im neunjährigem Gymnasium (G9) (Bayern) wurde der räumliche Bau
und das Reaktionsverhalten von Kohlenwasserstoffen mit Hilfe des Modells von der
Hybridisierung eingeführt, was die Bindungsverhältnisse über
 /
/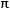 -Bindungen
erklärt.
-Bindungen
erklärt.
Durch die Einführung des achtjährigen Gymnasiums (G8) wurde der
Lehrplan in Chemie stark verändert. Dadurch änderte sich zum einen die
Jahrgangsstufe, in der die Organische Chemie gelehrt wird: die Schüler sind nun
mit 15-16 Jahren deutlich jünger. Zum anderen werden dem Lehrer wesentlich mehr
Freiheiten bei der Gestaltung des Unterrichts gegeben.
In diesem Zusammenhang
wurde z.B. die Festlegung auf das Hybridisierungs-Modell bei der Erläuterung der
Kohlenwasserstoffe aufgehoben. Das heißt nicht, dass die Verwendung des
Hybridisierungs-Modells und in dessen Folge die Erklärung von
Bindungsverhältnissen über
 /
/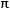 -Bindungen
verboten sind, aber es wurde der Weg frei gemacht für andere, möglicherweise
besser verständliche Modellvorstellungen.
-Bindungen
verboten sind, aber es wurde der Weg frei gemacht für andere, möglicherweise
besser verständliche Modellvorstellungen.
Eine vereinfachte Variante des Orbitalmodells ist das Kugelwolkenmodell nach
Kimball (1959), welches in den folgenden Arbeitsblättern verwendet wird. Dieses
Modell vernachlässigt die unterschiedliche Gestalt der s, p, d, f- Orbitalen und
stellt sie vereinfacht als Kugelwolken dar.Trotz dieser starken Vereinfachung
liefert dieses Modell für verschiedene atomare Größen z.B. Ionisierungsenergie,
Bindungslängen, Bindungsenergien erstaunlich gute Ergebnisse. Wissenschaftlich
hat es jedoch keine Bedeutung mehr. Für den Einsatz in der Schule ist es
aufgrund seiner Einfachheit und der dennoch guten Erklärung der Phänomene, die
in der Schule behandelt werden, sehr gut geeignet.
Da das Kugelwolkenmodell eine Vereinfachung des Atomorbitalmodells darstellt,
ist es auch ähnlich wie dieses aufgebaut. Im Zentrum jedes Atoms sitzt der
positiv geladene Atomkern, der als Punkt dargestellt wird. Für die
Elektronenhülle nimmt dieses Modell kugelförmige bis schwach ellipsoide
Ladungswolken an, die gemäß der Hundschen Regel mit Elektron en besetzt werden.
Für die K-Schale ist dies eine Kugelwolke. Für die zweite Periode werden vier
Kugelwolken angenommen, die sich wegen der Elektronenabstoßung möglichst weit
voneinander entfernen, was zu einer tetraedrischen Anordnung führt. Weitere
Perioden werden nach denselben Regeln aufgebaut.
Weiterführende Literatur:
-
Christen, H. R.; Einführung in die Chemie, 10. Aufl, Diesterweg/Salle,
Frankfurt a. M., 1975, S. 310f.
Voraussetzung:
Die Schüler sind mit dem Kugelwolkenmodell vertraut.
Bevor Sie mit dem Arbeitsblatt beginnen lesen sie die allgemeinen
technischen Voraussetzungen.
Die wichtigsten Ergebnisse der virtuellen Arbeitsblätter
können auf dem
Begleitblatt eingetragen werden, und bieten dadurch eine
Diskussionsgrundlage für den weiteren Unterricht.